- Prinsip Metode
Dalam medium alkali (pH = 11,7) dengan adanya natrium nitroferrike, amonia dan ion amonium dalam air bereaksi dengan ion salisilat dan hipoklorit untuk membentuk senyawa biru.
- Instrumen dan reagen
- Instrumen
– Spektrofotometer tampak (dilengkapi dengan kuvet 10 mm/30 mm).
- Reagen kunci
-Reagen yang Mengembangkan Warna (Salicylate-Potassium Sodium Tartrate Solution): Simpan dalam botol kaca coklat dengan stopper karet dalam gelap;
– Larutan Kerja Natrium Hipoklorit: Konsentrasi klorin tersedia 3,5 g/L, konsentrasi alkali bebas 0,75 mol/L (dihitung sebagai NaOH); simpan dalam botol tetes berwarna coklat; stabil selama 1 bulan.
– Larutan Natrium Nitroferisianida: 10 g/L; stabil selama 1 bulan.
- Solusi Standar:
– Larutan stok: 1000 μg/mL.
– Larutan antara: 100 μg/mL (stabil selama 1 minggu, disiapkan dengan mengencerkan 10,00 mL larutan stok menjadi 100 mL dalam labu ukur).
– Larutan kerja: 1 μg/mL (dibuat segar dengan mengencerkan 10,00 mL larutan antara hingga 1000 mL dalam labu ukur).
AKU AKU AKU.
- Persiapan sampel
- Pengumpulan dan pelestarian: Sampel disimpan dalam botol polietilen atau kaca.
-Pra-distilasi: Transfer 250 mL sampel air (atau sampel encer dengan kandungan nitrogen amonia tinggi, dibuat hingga 250 mL dengan air) ke dalam labu.
- Pengujian sampel
- Kurva kalibrasi:
- Untuk 10 mM cuvette: Siapkan seri standar dengan konten nitrogen amonia 0–8μg (lihat Tabel 1 dalam dokumen asli).
- Untuk 30 mm cuvette: Siapkan seri standar dengan isi nitrogen amonia 0–2μg (lihat Tabel 2 dalam dokumen asli).
- Setelah menambahkan reagen dan mengembangkan warna selama 60 menit, ukur absorbansi pada 697 nm.
– Pengukuran Sampel: Ambil 8,00 mL sampel air (atau sampel yang diencerkan jika konsentrasi nitrogen amonia > 1,0 mg/L) ke dalam kuvet 10 mL. Tambahkan 1,00 mL reagen pengembang warna, 2 tetes larutan natrium nitroferisianida, dan 2 tetes larutan kerja natrium hipoklorit. Campur, encerkan hingga tanda batas dengan air, dan kembangkan warna selama 60 menit. Ukur absorbansi pada 697 nm menggunakan jenis kuvet yang sama dengan kurva kalibrasi, dengan air sebagai referensi.
- Tes kosong: Ganti sampel air dengan air deionisasi dan ikuti prosedur yang sama untuk pretreatment dan pengukuran.
- Perhitungan hasil
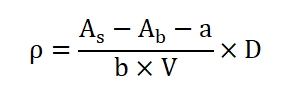
Di mana:
-Sebagai: Absorbansi sampel;
-Ab : Absorbansi tes kosong;
- A: Intercept of the Calibration Curve;
- B: Kemiringan kurva kalibrasi;
- V: Volume sampel uji (ML);
- D: Faktor pengenceran sampel air.
- Parameter metodologis
- Batas deteksi dan batas kuantisasi
- 10 mm cuvette:
– Batas deteksi laboratorium: 0,001 mg/L;
- Batas Kuantisasi Laboratorium: 0,004 mg/L.
- Cuvette 30 mm:
– Batas deteksi laboratorium: 0,001 mg/L;
- Batas Kuantisasi Laboratorium: 0,002mg/L.
- Presisi
– Untuk sampel standar dengan konsentrasi 0,477 mg/L dan 0,839 mg/L (n=10), deviasi standar relatif (RSD) masing-masing adalah 2,45% dan 1,07%, keduanya memenuhi persyaratan standar (≤2,94% dan ≤1,55%).
- Rentang linier
- 10 mm cuvette:
- Persamaan Linear: ABS = 9.24078c - 0,0099, r = 0,9996;
– Kisaran: 0–8μg (setara dengan 0–1,0 mg/L untuk sampel uji 8 mL).
- Cuvette 30 mm:
- Persamaan linier: ABS = 2.86547C + 0.02566, r = 0.9993;
– Kisaran: 0–2 μg (setara dengan 0–0,25 mg/L untuk sampel uji 8 mL).
- Tindakan pencegahan
- Kontrol secara ketat waktu pengembangan warna pada 60 menit dan hindari paparan cahaya untuk mempertahankan stabilitas reagen.
- Simpan solusi kerja hipoklorit natrium dan pengembangan warna reagen seperti yang ditentukan;
-Encerkan sampel air konsentrasi tinggi untuk memastikan absorbansi berada dalam kisaran linier kurva kalibrasi.

