La spectroscopie de fluorescence est un outil analytique puissant. Il’ commun dans les laboratoires scientifiques, les usines et les hôpitaux. Cette méthode examine la lumière émise par un matériau après qu'il absorbe de l'énergie. Elle offre des détails clairs sur cette matière. Mais “ fluorescence” couvre beaucoup de terrain. La technologie fonctionne à deux tailles très différentes: l'échelle moléculaire minuscule et l'échelle atomique encore plus petite.
Ce guide brosse d'abord l'idée principale. Ensuite, il plonge dans trois grandes façons de l'utiliser. Il’ Spectroscopie de fluorescence moléculaire, le choix habituel pour vérifier les molécules complexes. Ensuite, la spectroscopie par fluorescence à rayons X (XRF), un outil difficile pour repérer les éléments. Et enfin, la spectroscopie par fluorescence atomique (AFS), un moyen super-sensible de trouver certains éléments nocifs. Savoir comment chacun cour est la clé pour choisir le meilleur pour le travail.
Principes de la fluorescence
Le cœur de la fluorescence est simple. Un matériau absorbe de l'énergie et crache de la lumière. Un électron saute vers un point plus haut. Puis il retombe. Au cours du processus, il tire un photon. Cela’ S le glow. Qu’est-ce qui distingue ces méthodes ? Il’ c'est ce qui est excité - une molécule entière ou un seul atome. De plus, le type d'énergie utilisée pour démarrer les choses.
1. Spectroscopie de fluorescence moléculaire (en utilisant un spectrofluoromètre)
C'est la technique à utiliser lorsque les gens parlent de “ spectroscopie de fluorescence. ” Il’ est une grande affaire en biologie, le travail des matériaux et les études de santé.
Comment ça fonctionne au niveau moléculaire
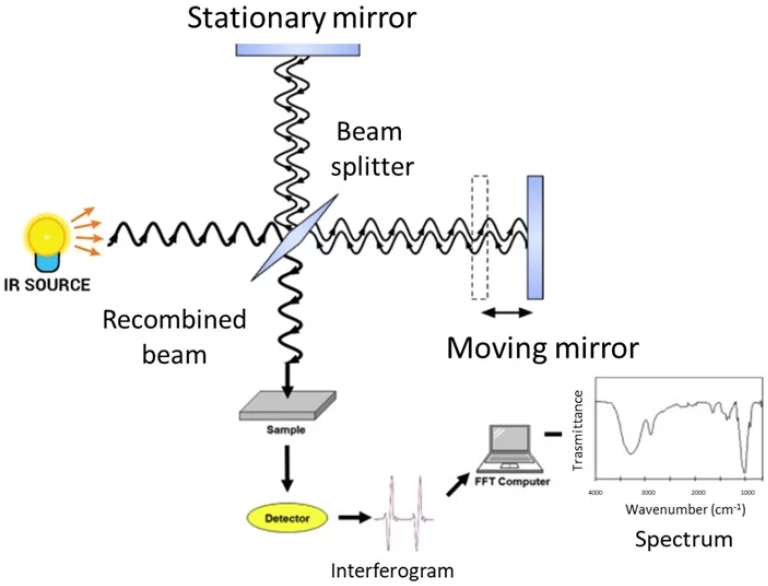
Imaginez ça. La méthode attrape la lumière UV ou visible à faible énergie, généralement entre 200 et 800 nanomètres. Cela frappe les électrons extérieurs dans une molécule. La molécule se refroidit et retombe à la normale. Il libère un photon avec une onde plus longue. Cela’ Les Stokes changent en action. Le modèle lumineux ? Il’ s comme une étiquette personnelle pour la molécule et son environnement. L'équipement ici est un spectrofluoromètre. Il comprend une lampe à xénon pour la lumière, des filtres pour trier les longueurs d'onde et un détecteur pointu comme un tube photomultiplicateur (PMT).
Ce qu'il détecte
- Molécules organiques et biologiquesIl cloue les choses qui s’allument, comme les colorants des plantes, les médicaments et les signes clés dans le corps tels que la protéine fluorescente verte (GFP).
Il repère ces choses rapidement. Sensibilité ? Jusqu'à des niveaux nanomolaires, ou 10 ⁻⁹ M. Cela’ S minuscule.
- Interactions moléculaires: Cet outil ressent des changements dans une molécule’ Le monde s. La force de luminosité change avec le type de liquide, le niveau d'acide ou les bulles d'air. Alors il’ Parfait pour regarder les protéines se torder, les enzymes accélérer les réactions, ou les liens se forment entre les partenaires. Qu’ En outre, il gère des contrôles réguliers pour les quantités ou ceux basés sur le temps pour les danses rapides - nanosecondes à picosecondes.
Tout d'abord, la fluorescence à l'état stable saisit simplement la luminosité moyenne pour compter les molécules. Temps résolu ? Il suit comment la lumière s'estompe. Cela révèle des mouvements cachés dans les choses.
2. Fluorescence au niveau atomique : deux techniques distinctes
Changez les engrenages maintenant. Quand vous’ après des atomes simples - pas des molécules agrégées - l'approche se retourne. Deux voies principales s'éloignent ici.
2.1. Spectroscopie par fluorescence à rayons X (XRF)
Le XRF prend un coup de poing. Il’ s non-dommageable et idéal pour comprendre ce que’ s dans un échantillon au niveau des éléments.
Comment ça fonctionne au niveau atomique
Oubliez la lumière douce. Cela utilise des rayons X de 1 à 100 keV. Le faisceau éclate un électron libéré d'un atome’ s coquille de noyau. Alors ? Un électron extérieur glisse pour le réparer. Boom — un nouveau rayon X apparaît comme “ fluorescence. ” Ce ray’ S puissance ? Il’ s un cadeau mort pour l'élément.
Ce qu'il détecte
- Composition élémentaireLa radiographie XRF balaie rapidement les éléments de base, du magnésium (Mg) ou de l'aluminium (Al) jusqu'à l'uranium (U). Il capture des traces en ppm - parties par million. La grande question à laquelle il répond : “ Qu’ est le maquillage de ce truc, élément sage? ”
En outre, il’ s pratique pour les solides ou les poussières. Aucune préparation nécessaire.
- Applications: Pensez aux magasins de métal vérifiant 316 lots d'acier inoxydable. Ou les chiens de roche cartographiant les couches de terre. Même les chiens de garde sniffer du plomb dans la vieille peinture. Ainsi, il convient aux contrôles de qualité, aux sciences de la terre et aux efforts de montre verte.
2.2. Spectroscopie par fluorescence atomique (AFS)
AFS va en profondeur. Il’ s picky et super nette pour seulement une poignée d'éléments.
Comment ça fonctionne au niveau atomique
Étape 1: Découpez l'échantillon. Plus de liens moléculaires, seulement des atomes libres dans un nuage de gaz. Cela’ atomisation. Ensuite, une lumière ciblée - comme d'une lampe cathodique creuse - déclenche l'onde exacte pour réveiller seulement les atomes souhaités. Ils s'éclairent en réponse. Un détecteur saisit ce signal pur. L'installation ? Spectromètre de fluorescence atomique.
Ce qu'il détecte
- Éléments toxiques spécifiques: AFS est’ T pour tout. Il brille à des chasses ultra-basses à des poisons comme l'arsenic (As), le mercure (Hg), le sélénium (Se) et le cadmium (Cd). Des limites ? ppb ou même ppt, en fonction de la cible et du mélange.
Donc, il’ Surkill pour la plupart. Mais ça’ s le point - répond à des règles difficiles.
- ApplicationsLes contrôles alimentaires sont en haut de la liste. Pensez à scanner le poisson pour le mercure sous la FDA’ s 1,0 ppm cap. Des tests environnementaux aussi. Il bat les autres outils en termes de netteté, de sorte que la conformité est facile.
Résumé et comparaison
| Fonctionnalité | Fluorescence moléculaire | Fluorescence par rayons X (XRF) | Fluorescence atomique (AFS) |
|---|---|---|---|
| Cible principale | Molécules | Atomes (large portée) | Atomes (peu spécifiques) |
| Source d'excitation | Lumière visible UV | Rayons X | Lumière de longueur d'onde spécifique |
| Etat de l'échantillon | Solution généralement liquide | Solide, poudre ou liquide | L'échantillon est atomisé en gaz |
| Informations | Structure moléculaire, concentration | Composition élémentaire | Concentration d'éléments ultra-traces |
| Cas d'utilisation clé | Recherche biologique, pharma | Contrôle qualité, géologie | Sécurité alimentaire, essais environnementaux |
Remarque rapide : Chaque ligne met en évidence la division. Le côté moléculaire reste mouillé et vibroux. Les atomiques ? Faits secs ou nuages de gaz.
Instrumentation d'un fabricant de confiance: PERSEE
Choisir le bon équipement une tonne d'importance. Associez-le à l'échelle - molécules ou atomes. Un constructeur solide comme Persan couvre toutes les bases.
Pour ces chasses aux atomes toxiques, PERSEE construit Spectromètres de fluorescence atomiqueIls’ réajusté strictement pour les règles alimentaires et écologiques. Pas de raccourcis.

Conclusion
Les trois s'appuient sur la luminosité fluorescente. Mais leurs emplois ? Nuit et jour. Choisissez en fonction de votre puzzle. Vous voulez déballer les molécules enchevêtrées et leurs chats? Prenez la fluorescence moléculaire. Besoin de la ligne d'éléments bruts en un morceau? Règles XRF. Pour identifier des traces d'atomes toxiques ? AFS gagne les mains.
Questions fréquentes :
Q1: Quelle est la différence entre la fluorescence et la phosphorescence?
A : Les deux démarrent des coups d'énergie et de la lumière. Mais la phosphorescence le traîne. Des trajets d'électrons plus lents signifient des lumières qui persistent - des secondes ou des minutes, comme des baguettes de lumière. La fluorescence ? Il’ S rapide. Nanosecondes seulement.
Q2: La spectroscopie de fluorescence peut-elle détecter les métaux?
A : Bien sûr. Mais cela dépend du style. La radiofréquence XRF repère les atomes métalliques directement vers le haut. AFS cloue certains comme le mercure et le cadmium à des niveaux de chuchotement. La fluorescence moléculaire saute les coups directs. Au lieu de cela, il utilise des sondes intelligentes, des molécules qui ne brillent que lorsqu'elles attrapent ce métal.
Q3: Pourquoi un échantillon est transformé en gaz pour AFS mais pas pour XRF?
A : AFS exige des atomes libres sous forme de gaz. De cette façon, la lampe’ La lumière n'atteint que la cible sans encombrement moléculaire. XRF ? Ces rayons X traversent facilement les solides ou les liquides. Ils secouent les électrons intérieurs, quelle que soit la configuration. Aucun gaz nécessaire.